艾伟拓(上海)医药科技有限公司
12 年
手机商铺
- NaN
- 0.7999999999999998
- 1.7999999999999998
- 0.7999999999999998
- 3.8
推荐产品
新闻中心/正文
皂苷类佐剂:实现疫苗安全与免疫的双重突破
1586 人阅读发布时间:2025-04-27 13:33
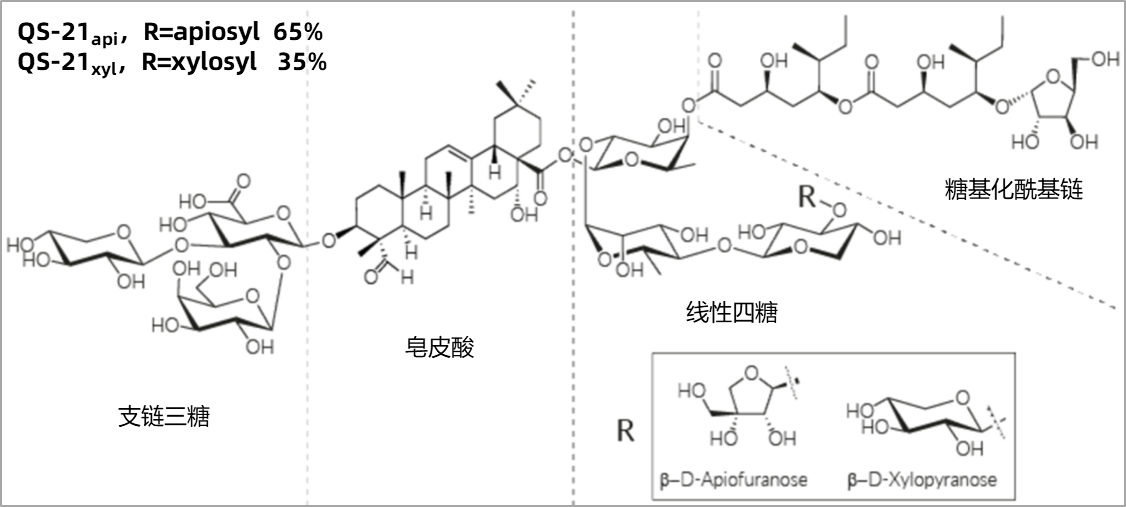
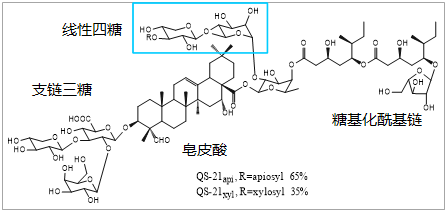
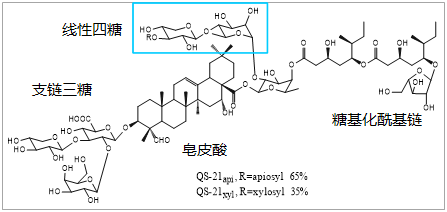
QS-21是一种天然来源的皂苷类疫苗佐剂,主要从皂树(Quillaja saponaria)的树皮中提取。它是一种三萜糖苷,由一个中心三萜核心(quillaic acid),一个分支的三糖基(分支糖链),一个线性四糖基(末端糖基),以及一个通过酯键连接的酰基侧链组成。QS-21的主要异构体包括QS-21-Api(D-呋喃糖)和QS-21-Xyl(D-吡喃木糖),两者的比例为65:35。
QS-21具有显著的免疫刺激活性,能够同时激活体液免疫和细胞免疫,增强抗体生成和特异性T细胞反应,包括Th1和Th2免疫反应。它能够刺激树突状细胞的激活,促进IgG1和IgG2a抗体的产生,并诱导干扰素-γ(IFN-γ)的分泌。此外,QS-21还能够增强细胞毒性T细胞(CTL)的功能,从而对抗多种传染病和癌症。
然而,传统QS-21因提取工艺的限制面临产能与纯度双重制约,AVT通过自主开发的分离技术体系,成功实现从皂树全植株中高效获取高纯度QS-21,并建立了稳定、可靠、通用于定量的分析方法,可实现日常质控,分离分析组分含量,从而加快研发和问题溯源的流程。
AVT QS21优势:
AVT利用独有的分离纯化技术平台同步分离出QS-7、QS-18等组分。在疫苗佐剂领域,QS-7 作为三萜糖苷类新型佐剂也备受关注。它融合了低毒性与高效免疫激活两大核心优势,在安全性与有效性间实现了出色平衡。QS-7 与QS-21具有相同的母核结构,但其糖基化程度显著提升,脂肪酰基单元明显缩短[1],QS-7通过 C-28 位糖基化修饰和乙酰基取代结构,在保留与 QS-21 相当的免疫刺激活性(如增强 Th1/Th2 平衡反应和 CTL 生成)的同时,降低溶血性,提升了安全性,为疫苗研发提供了更可靠的佐剂选择方案。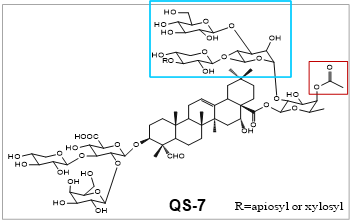
QS-7 目前已作为核心成分应用于 Matrix-M 佐剂系统,并在两款人用重组疫苗中实现上市应用——Novavax 的 COVID-19 疫苗 NVX-CoV2373 与印度血清研究所的R21/Matrix-M 疟疾疫苗。
Novavax 研发的蛋白亚单位疫苗 NVX-CoV2373,含融合前稳定刺突蛋白(BV2373)及基于皂苷的 Matrix-M™佐剂,作为全球首获批的 COVID-19 蛋白疫苗平台,其对 SARS-CoV-2 感染的保护效力与 mRNA 疫苗相当,且相较明矾等传统佐剂,展现出更优的抗体应答水平。
由英国牛津大学詹纳研究所与印度血清研究所联合开发的 R21/Matrix-M 疟疾疫苗,是继 RTS,S/AS01 后第二款获世界卫生组织(WHO)认可的疟疾疫苗。临床试验数据显示,该疫苗在不同流行区域均表现出 75% 的保护效力,尤其显著降低了儿童群体中症状性疟疾的发生率。因其兼具良好的安全性与耐受性,生产工艺易于规模化放大且成本可控,成为资源受限地区疟疾防控的重要工具。
Matrix-M佐剂是一种基于皂苷的佐剂,能够增强免疫反应,使疫苗更高效和持久,由两个单独的皂苷组分(42.5 μg Fraction-A + 7.5 μg Fraction-C)制备而成,使用胆固醇和磷脂作为稳定剂[2]。其中,Fraction-C 以 QS-21 为主要成分,具备强大免疫刺激活性,但在小鼠模型中存在反应原性;Fraction-A 主要为QS-7[3],同等剂量下免疫增强效应弱于 Fraction-C,却具有更高的动物耐受性。二者经优化组合后,在保留高免疫刺激能力的同时,显著降低了动物模型中的反应原性。部分研究提及 Matrix-M 佐剂中或含 QS-17 成分[4、5],但尚无官方文件明确披露其具体组分,其实际构成仍需进一步研究验证。
除已上市的两款疫苗外,当前全球已有十余项相关项目进入临床阶段,应用方向更拓展至重组治疗性疫苗领域。随着 Matrix-M 佐剂应用场景的持续扩大, QS-7 的研究与开发将迎来更广泛的关注。
QS-18 作为皂树皮中含量最高的天然皂苷提取物,具有与QS-21相似的结构,会与细胞膜胆固醇相互作用从而引起细胞毒性,长期以来受限于细胞毒性而导致其应用一直被忽视。2024 年,纽约州立大学布法罗分校生物医学工程系 Jonathan F. Lovell 团队在《Nature Biomedical Engineering》发表的研究成果证实了QS-18的安全性。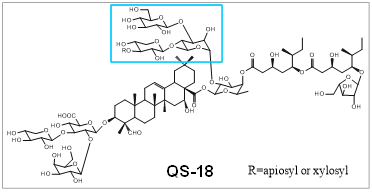
该研究表明,QS-18 可与 QS-21 一样自发插入含磷酸化六酰基二糖(PHAD)和胆固醇的 CoPoP/PHAD 脂质体结构中,通过脂质体的物理包封能中和其溶血活性(图1 A);在小鼠模型中,含 QS-18 的脂质体疫苗经脚掌注射后,未观察到局部红肿、硬结等反应原性表现(图1 B);相比不含QS-18的脂质体疫苗佐剂系统,QS-18并没有引起显著更多的体重减轻(图1 C)。除此之外,注射两天后并未引起炎症细胞因子升高,具有良好安全性(图1 D)[6]。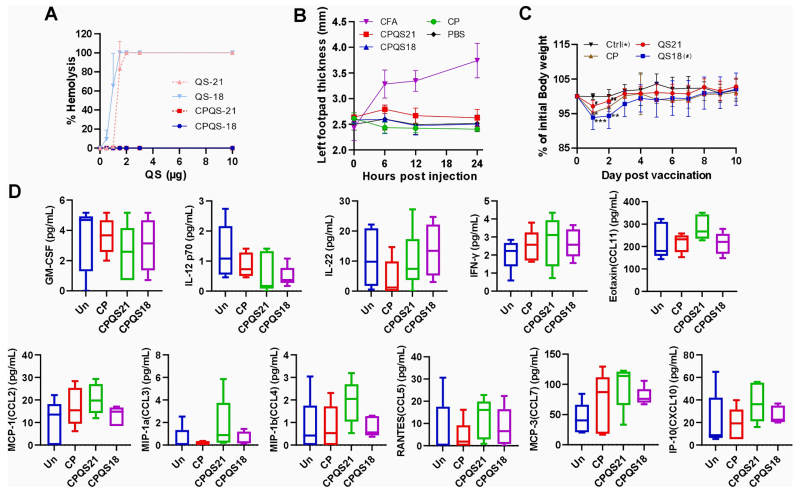
图1:(A) 中和溶血活性; (B) 注射后脚掌厚度变化; (C) 单次注射后小鼠的体重变化;(D) 单次注射后小鼠血清细胞因子浓度
备注:CoPoP/PHAD/QS-21(CPQS-21)、CoPoP/PHAD/QS-18(CPQS-18)
在免疫激活机制方面,QS-18 与抗原肽的配位结合效率与 QS-21 无统计学差异,且在肿瘤疫苗模型中表现出更优的细胞免疫诱导能力。实验数据显示,与 QS-21 脂质体相比,QS-18 递送的肽疫苗可诱导更高水平的肿瘤新抗原特异性和肿瘤相关抗原特异性CD8+ T细胞,同时未检测到更高的毒性[6]。
因此,含有QS-18的脂质体是一种安全有效的佐剂,由于其天然高丰度特性(占皂树皮提取物的 35%),使其规模化生产成本较 QS-21低,为资源受限地区的疫苗普及提供了经济可行性,不仅为现有皂苷佐剂体系提供了低成本替代方案,更为开发新一代高效、安全的肿瘤及传染病疫苗奠定了基础。
参考文献:
【1】 Kensil CR, Wu JY, et al. QS-21 and QS-7: purified saponin adjuvants. Dev Biol Stand. 1998;92:41-7.
【2】 Magnusson SE, Altenburg AF, et al. Matrix-M™ adjuvant enhances immunogenicity of both protein- and modified vaccinia virus Ankara-based influenza vaccines in mice. Immunol Res. 2018 Apr;66(2):224-233.
【3】Bengtsson, K. L.. Matrix M Adjuvant Technology. Novel Immune Potentiators and Delivery Technologies for Next Generation Vaccines, 2012,309–320.
【4】Reed J, Orme A, et al.Elucidation of the pathway for biosynthesis of saponin adjuvants from the soapbark tree. Science. 2023 Mar 24;379(6638):1252-1264.
【5】Martin LBB, Kikuchi S, et al. Complete biosynthesis of the potent vaccine adjuvant QS-21. Nat Chem Biol. 2024 Apr;20(4):493-502.
【6】Zhou S, Song Y, et al. The predominant Quillaja Saponaria fraction, QS-18, is safe and effective when formulated in a liposomal murine cancer peptide vaccine. J Control Release. 2024 May;369:687-695.
AVT独有的分离纯化技术平台已成功分离出QS-21、QS-7、QS-18等组分,为疫苗研究提供更完整的QS系列选择;针对兽用疫苗领域,我们也推出了高纯度的QS-ANM,满足更高安全标准需求;并提供定制产品QS-17。依托于分离技术平台优势,AVT现已具备QS全系列产品供应能力,并支持客户定制化开发,助力疫苗研发进程。
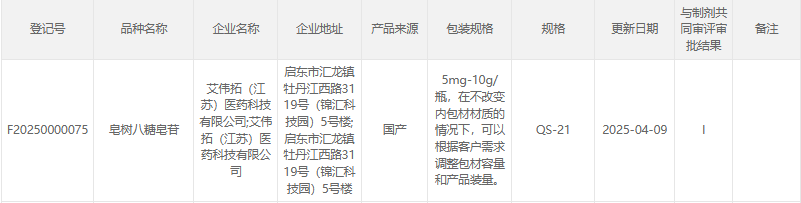
2025年04月09日,艾伟拓皂树八糖皂苷(QS-21)在国家药审中心原辅包登记平台完成备案并公示。